Amoni Clorid: Ứng Dụng Đa Năng Trong Y Tế, Công Nghiệp và Những Lưu Ý Khi Sử Dụng
Amoni Clorid (NH₄Cl) là hợp chất hóa học đa dụng, ứng dụng trong y tế, công nghiệp và nông nghiệp. Bài viết tổng hợp chi tiết về công dụng, cơ chế tác động, tác dụng phụ và hướng dẫn sử dụng an toàn.
Amoni Clorid là gì?
Tính chất hóa học và vật lý
Ứng dụng trong y tế
Ứng dụng trong công nghiệp
Vai trò trong nông nghiệp
Tác dụng phụ và rủi ro
Hướng dẫn sử dụng an toàn
Tương tác thuốc và cảnh báo
Nghiên cứu mới và xu hướng
Kết luận
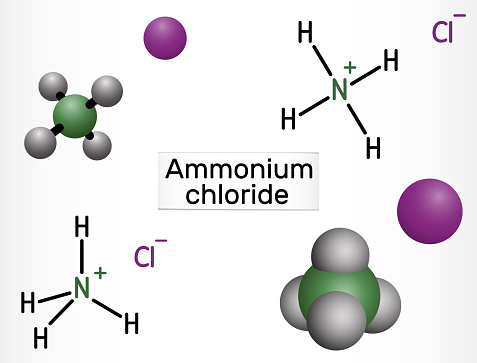
Amoni Clorid (NH₄Cl), còn gọi là muối amoni, là hợp chất vô cơ gồm amoni (NH₄⁺) và clorua (Cl⁻). Đây là chất rắn kết tinh màu trắng, không mùi, dễ tan trong nước và có vị mặn lạnh.
Nguồn gốc: Được điều chế từ phản ứng giữa amoniac (NH₃) và axit clohidric (HCl).
Phân bố: Tồn tại tự nhiên trong khoáng vật sal ammoniac, nhưng chủ yếu được sản xuất công nghiệp.
Dạng bào chế: Bột, viên nén, dung dịch tiêm, hoặc kết hợp trong các sản phẩm công nghiệp.
Khối lượng phân tử: 53.49 g/mol.
Độ tan: Tan tốt trong nước (37.2g/100ml ở 20°C), ít tan trong ethanol.
Nhiệt độ nóng chảy: 338°C (phân hủy thành NH₃ và HCl khi đun nóng).
Tính axit yếu: Dung dịch nước có pH ~4.5–6.
Phản ứng với kiềm:
NH₄Cl + NaOH → NH₃ + H₂O + NaCl
Phản ứng nhiệt phân:
NH₄Cl → NH₃↑ + HCl↑
Cơ chế: Bổ sung ion Cl⁻, trung hòa lượng bicarbonate dư thừa trong máu.
Liều dùng: 1–2g/ngày (uống hoặc tiêm tĩnh mạch), tùy mức độ bệnh.
Cơ chế: Kích thích tiết dịch phế quản, làm loãng đờm, dễ ho khạc.
Dạng dùng: Kết hợp trong siro ho hoặc viên ngậm.
Dùng trong trường hợp mất Cl⁻ do nôn mửa, tiêu chảy.
Vai trò: Chất điện phân trong pin kẽm-carbon, giúp dẫn điện.
Mạ kẽm: Làm sạch bề mặt kim loại trước khi mạ.
Hàn thiếc: Tạo môi trường axit nhẹ để hàn dính.
Cố định thuốc nhuộm: Giúp màu bám chắc vào vải.
Bảo quản da sống: Ức chế vi khuẩn phân hủy.
Cung cấp nitơ và clo cho cây trồng, phù hợp với đất kiềm.
Cải tạo đất: Giảm pH đất kiềm, tăng khả năng hấp thụ dinh dưỡng.
Phân bón: Kết hợp với NPK để bổ sung clo, ngăn ngừa thiếu hụt vi lượng.
Da/mắt: Gây kích ứng, mẩn đỏ.
Hít phải bột: Ho, khó thở, viêm phế quản.
Triệu chứng: Buồn nôn, nôn, co giật, rối loạn điện giải (tăng Cl⁻ máu).
Xử lý: Ngừng thuốc, truyền dịch cân bằng ion.
Thủy sinh: Nồng độ cao gây độc cho tôm, cá.
Trong y tế:
Tuân thủ liều lượng của bác sĩ.
Tránh dùng cho người suy thận, nhiễm toan.
Trong công nghiệp:
Đeo găng tay, kính bảo hộ.
Bảo quản nơi khô ráo, tránh nhiệt độ cao.
Thuốc lợi tiểu: Tăng nguy cơ mất kali.
Corticosteroid: Làm trầm trọng tình trạng giữ nước.
Chống chỉ định: Bệnh nhân suy gan, thận nặng.
Pin thể rắn: Thử nghiệm NH₄Cl làm chất điện phân thân thiện môi trường.
Nông nghiệp hữu cơ: Ứng dụng cải thiện dinh dưỡng đất mà không gây ô nhiễm.
Thay thế hóa chất độc hại: Dần thay thế NH₄Cl trong một số quy trình công nghiệp.
Amoni Clorid là hợp chất linh hoạt, đóng vai trò quan trọng trong y tế, công nghiệp và nông nghiệp. Tuy nhiên, cần sử dụng đúng cách để tránh tác dụng phụ và rủi ro sức khỏe. Người dùng nên tham khảo ý kiến chuyên gia và tuân thủ hướng dẫn an toàn.
Amoni Clorid
Ứng dụng Ammonium Chloride
Tác dụng phụ Amoni Clorid
Cách dùng Amoni Clorid an toàn
Amoni Clorid trong công nghiệp

