 Hộp 1 chai x 500ml
Hộp 1 chai x 500ml Túi 3 ngăn
Túi 3 ngănSodium Acetate: Công Thức, Ứng Dụng Đa Ngành Và Lưu Ý Khi Sử Dụng
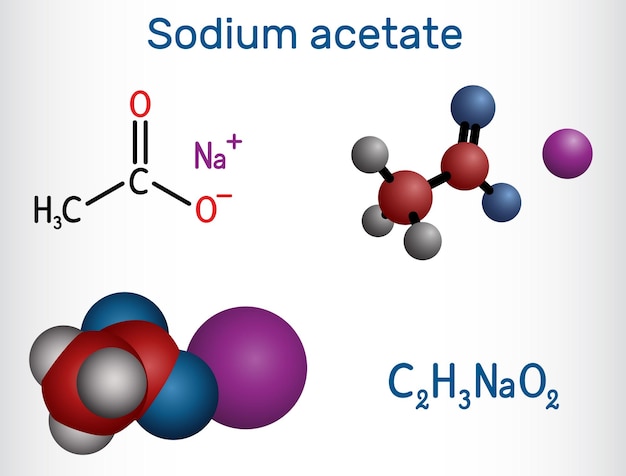
Khám phá Sodium Acetate – muối natri đa năng trong công nghiệp, thực phẩm và y tế. Tìm hiểu cấu trúc hóa học, công dụng, độ an toàn và xu hướng ứng dụng bền vững.
Sodium Acetate (CH₃COONa) là muối natri của axit acetic, tồn tại ở dạng khan hoặc ngậm nước (trihydrat). Với khả năng điều chỉnh pH, tạo đệm và phản ứng nhiệt lạnh, nó được ứng dụng rộng rãi từ sản xuất thực phẩm đến xử lý môi trường. Bài viết phân tích chi tiết cấu trúc, công dụng, và những tranh cãi xung quanh hoạt chất này.
Công thức hóa học:
Dạng khan: CH₃COONa.
Dạng trihydrat: CH₃COONa·3H₂O.
Tính chất vật lý:
Màu sắc: Tinh thể trắng, không mùi.
Độ tan: 46.4 g/100 mL nước (20°C).
Điểm nóng chảy: 324°C (dạng khan), 58°C (dạng trihydrat).
Khả năng đệm pH: Duy trì pH ổn định (4.5–5.5) khi kết hợp với axit acetic.
Phân hủy nhiệt:
Khi đun nóng trên 324°C → Natri cacbonat (Na₂CO₃) + Axeton (CH₃COCH₃).
Phản ứng nhiệt lạnh:
Dung dịch bão hòa kết tinh → Giải phóng nhiệt (exothermic).
Chất bảo quản (E262i, E262ii): Ngăn vi khuẩn, nấm mốc trong bánh mì, snack.
Điều chỉnh độ chua: Cân bằng vị chua trong nước sốt, dưa chua.
Tạo hương vị: Tăng vị mặn gián tiếp trong khoai tây chiên.
Dung dịch đệm truyền tĩnh mạch: Điều trị nhiễm toan do tiểu đường hoặc sốc.
Thành phần thuốc giảm đau: Kết hợp với Paracetamol để tăng độ hòa tan.
Khử kim loại nặng: Kết tủa chì (Pb²⁺), đồng (Cu²⁺) trong nước thải công nghiệp.
Bể đệm sinh học: Kiểm soát pH trong hệ thống xử lý nước.
Sản xuất cao su tổng hợp: Chất xúc tác trong quá trình polymer hóa.
Tạo bọt cứu hỏa: Thành phần của bột chữa cháy khô (đặc biệt ở dạng trihydrat).
Dung dịch đệm: Duy trì pH ổn định trong phản ứng sinh hóa.
Túi sưởi hóa học: Dung dịch bão hòa Sodium Acetate tạo nhiệt khi kết tinh.
An toàn và thân thiện: Được FDA công nhận là phụ gia thực phẩm GRAS (Generally Recognized As Safe).
Chi phí thấp: Dễ tổng hợp từ axit acetic và natri bicarbonate.
Linh hoạt: Sử dụng được trong đa dạng môi trường (axit, kiềm, nhiệt độ cao).
Tiếp xúc da: Kích ứng nhẹ, đặc biệt với da nhạy cảm.
Tiêu thụ quá liều: Gây buồn nôn, tăng natri máu (hiếm).
Môi trường: Xả thải nồng độ cao → Tăng độ mặn đất và nước.
Trong thực phẩm: Giới hạn 0.1–0.3% tùy sản phẩm (theo WHO).
Xử lý hóa chất: Đeo găng tay, kính bảo hộ khi làm việc với dạng bột.
| Hoạt Chất | pH Đệm | Ưu Điểm | Nhược Điểm |
|---|---|---|---|
| Sodium Acetate | 4.5–5.5 | Giá rẻ, dễ tổng hợp | Hiệu quả giảm ở nhiệt độ cao |
| Tris-HCl | 7.5–9.0 | Ổn định với enzyme | Đắt tiền, độc với tế bào |
| Phosphate | 6.0–8.0 | Phổ rộng | Gây ô nhiễm nguồn nước |
Tranh cãi: Sodium Acetate có thể làm tăng lượng natri nạp vào, ảnh hưởng đến tim mạch.
Giải pháp: Thay thế bằng kali acetate (E261) cho người huyết áp cao.
Phân hủy sinh học chậm: Cần xử lý nước thải chứa Sodium Acetate bằng phương pháp điện hóa.
Sản xuất từ nguồn tái tạo: Lên men vi sinh để tạo axit acetic từ phế phẩm nông nghiệp.
Ứng dụng trong pin nhiên liệu: Sodium Acetate làm chất điện phân thân thiện.
Vật liệu thông minh: Túi sưởi tái sử dụng từ dung dịch Sodium Acetate.
Q: Sodium Acetate có gây ung thư không?
A: Không! Cơ quan Nghiên cứu Ung thư Quốc tế (IARC) xếp Sodium Acetate vào nhóm 3 – không gây ung thư.
Q: Có thể tự làm Sodium Acetate tại nhà?
A: Có! Trộn giấm (axit acetic) với baking soda (natri bicarbonate) → Lọc và cô đặc.
Q: Sodium Acetate và Sodium Diacetate khác nhau thế nào?
A: Sodium Diacetate (E262ii) là hỗn hợp Sodium Acetate và axit acetic, có tính kháng khuẩn mạnh hơn.
Sodium Acetate là hoạt chất đa năng, góp mặt trong hầu hết lĩnh vực đời sống nhờ tính an toàn và hiệu quả. Dù tồn tại một số tranh cãi, việc nghiên cứu ứng dụng bền vững và tuân thủ liều lượng sẽ phát huy tối đa tiềm năng của hợp chất này.
Lưu ý: Sodium Acetate, công thức Sodium Acetate, ứng dụng Sodium Acetate, Sodium Acetate trong thực phẩm, tác dụng phụ Sodium Acetate.
Bài viết kết hợp thông tin khoa học, giúp độc giả nắm bắt toàn diện về Sodium Acetate từ lý thuyết đến thực tiễn.

